Profesional:Publicaciones
miércoles, 5 de mayo de 2021
martes, 11 de mayo de 2021

El Hipotiroidismo es causado por una disminución hormonal de la glándula tiroides, las causas más frecuentes es por déficit de yodo y por tiroiditis autoinmune. Su presentación puede ser desde la manera asintomática, hasta cuadros graves que ponen en riesgo la vida del paciente. La sintomatología puede ser inespecífica por lo que pueden pasar casos inadvertidos. En la mayoría de casos el tratamiento es de por vida.
El hipotiroidismo es un síndrome producido por disminución de la producción hormonal de la glándula tiroides necesarias para satisfacer las demandas metabólicas del cuerpo.
En general el hipotiroidismo primario se debe a una enfermedad intrínseca de la glándula tiroides, caracterizada por presentar valores disminuidos de tiroxina (T4) con concentraciones elevadas de tirotropina (TSH).
El hipotiroidismo no tratado puede contribuir a la hipertensión, dislipidemia, infertilidad, deterioro cognitivo y disfunción neuromuscular.
Epidemiología
Es la segunda enfermedad de causa endocrina más frecuente. A nivel mundial la prevalencia de hipotiroidismo primario varía entre 0.1 a 2% y es 10 veces más frecuente en mujeres que en hombres. Aumentando un 7-10% en mayores de 60 años. En mujeres embarazadas se ha reportado hipotiroidismo clínico en 0.2 a 0.5% y 2 a 2.5% en hipotiroidismo subclínico.
El hipotiroidismo es más común en pacientes con enfermedades autoinmunes como diabetes mellitus tipo 1, atrofia gástrica autoinmune y enfermedad celiaca, puede ocurrir como parte de múltiples enfermedades autoinmunes.
Las personas con síndrome de Down o síndrome de Turner tienen un mayor riesgo de padecerla, por el contrario, el tabaquismo y la ingesta moderada de alcohol se asocian con un riesgo reducido. Los trastornos autoinmunitarios de la glándula toroides pueden estimular la sobreproducción de hormonas tiroideas o producir destrucción glandular y deficiencia hormonal.
Anatomía
La tiroides tiene dos lóbulos conectados por un istmo que se encuentra delante de la tráquea, entre el cartílago cricoides y la escotadura supraesternal, Pesa de 12 a 20 g, es muy vascularizada y tiene consistencia blanda.
Posterior de cada uno de los cuatro polos de la tiroides se localiza la glándula paratiroidea que produce la hormona paratiroidea. Los nervios laríngeos recurrentes atraviesan los bordes laterales de la glándula tiroidea y deben identificarse durante la cirugía tiroidea para evitar paralipsis de las cuerdas vocales.
Regulación del eje tiroideo
La TRH (hormona liberadora de tirotropina) hipotalámica estimula la producción de TSH (hormona estimulante de la tiroides) que a su vez, estimula la síntesis y secreción de hormonas tiroideas. La glándula tiroidea normal produce dos hormonas tiroideas: tiroxina o T4 y triyodotironina oT3. Aunque T4 se produce en mayores cantidades, la T3 es la forma biológicamente activa. Aproximadamente el 80 % de la T3 se deriva de la conversión periférica de T4 por las enzimas desyodasas.
La TSH secretada por las células tirotropas de la adenohipófisis desempeña una función crucial en el control del eje tiroideo y es el mejor marcador fisiológico de la acción de las hormonas tiroideas.
Las hormonas tiroideas actúan principalmente a través de receptores de hormona tiroidea por retroalimentación negativa inhibiendo la producción de TRH y TSH. La TRH es el regulador positivo principal de la síntesis y secreción de TSH, es decir la concentración reducida de hormona tiroidea aumenta la producción basal y potencia la estimulación de TSH mediada por TRH.
Las concentraciones elevadas de hormona tiroidea suprimen de forma rápida y directa la secreción de expresión del gen e inhiben el estímulo de la TSH mediada por la TRH, indicando que la hormona tiroidea son las reguladoras principales de la producción de TSH.
La TSH se libera de manera pulsátil, alcanzando su nivel máximo por la noche. Con la TSH baja o alta, se debe cuantificar los niveles de hormona tiroidea para establecer el diagnóstico de hipotiroidismo o hipertiroidismo. Cuando se libera, las hormonas tiroideas se combinan inmediatamente con proteínas plasmáticas. La globulina fijadora de tiroxina capta la mayoría de las hormonas liberadas uniéndose con más facilidad la tiroxina. La menor afinidad de la triyodotironina por las proteínas puede justificar su mayor rapidez de acción y su mayor brevedad.
Un método indirecto que se utiliza con menor frecuencia para calcular las concentraciones de hormona tiroidea libre consiste en calcular el índice de T3 o T4 libre a partir de la concentración total de T4 o de T3 y la proporción de unión de hormonas tiroideas a proteínas THBR. (Thyroid Hormone Binding Ratio).
El producto de THBR y la T3 o T4 proporciona un índice que corrige las concentraciones totales anómalas de hormona causadas por defectos de la unión con la proteína.
Las concentraciones totales de hormona tiroidea están elevadas cuando la TBG (globulina fijadora de tiroxina) está incrementada debido a los estrógenos (embarazo, uso de anticonceptivos orales, tratamiento hormonal, tamoxifeno, enfermedad inflamatoria hepática) y reducidos cuando la unión a TBG está disminuida (andrógenos, síndrome nefrótico). Los trastornos genéticos y las enfermedades agudas también pueden causar anomalías de las proteínas transportadoras de hormonas tiroideas y diversos fármacos (fenitoína, carbamazepina, salicilatos y antiinflamatorios no esteroideos) también pueden interferir con su unión a las hormonas tiroideas.
El hipotiroidismo se puede clasificar en primario debido a deficiencia de hormona tiroidea, secundaria debido a deficiencia de TSH y terciaria debido a deficiencia de hormona liberadora de tirotropina o TRH y extratiroidea o periférica.
Al actuar por medio de los receptores nucleares α y β, estas hormonas desempeñan una función fundamental en la diferenciación celular durante el desarrollo y ayudan a conservar las homeostasis termógena y metabólica en el adulto.
Clasificación
Primario:
Se da por afectación tiroidea, como causas están la tiroiditis crónica autoinmune (enfermedad de Hashimoto) otros tipos de tiroiditis, tiroidectomía total o subtotal, tratamiento con yodo, excesivo aporte de yodo (uso de amiodarona o medios de contraste yodado).
Secundario:
Debido a la deficiencia o falta de secreción de TSH por la adenohipófisis, habitualmente un hipopituitarismo como tumor de silla turca o enfermedades infiltrativas.
Terciario.
Debido a déficit de la TRH por alteración hipotalámica o lesiones del tallo hipofisiario.
Hipotiroidismo primario
La deficiencia de yodo es la causa más importante en el mundo. En áreas donde no hay problemas de ingesta de yodo, la causa que predomina es la tiroiditis autoinmune crónica o enfermedad de Hashimoto. En la mayoría de los pacientes con tiroiditis autoinmune están presentes concentraciones elevadas de anticuerpos antitiroideos, predominantemente anticuerpos de peroxidasa tiroidea y anticuerpos antitiroglobulina.
Los fumadores tienen concentraciones más bajas de anticuerpos contra peroxidasa tiroidea que los no fumadores y la incidencia de tiroiditis autoinmune aumenta después de dejar de fumar.
Otros factores ambientales implicados en la tiroiditis autoinmune es la deficiencia de vitamina D, selenio y la ingesta moderada de alcohol. El yodo es un componente esencial de la hormona tiroidea, la deficiencia de yodo puede provocar bocio, nódulos tiroideos e hipotiroidismo, la consecuencia más grave de la deficiencia de yodo es el cretinismo. A pesar de los programas de fortificación con yodo como una intervención en salud pública, todavía afecta a partes de África, Asia y países de bajos ingresos.
Fármacos que tienen yodo como la amiodarona pueden restringir la producción de hormona tiroidea bloqueando inmediatamente la síntesis de hormona tiroidea (efecto Wolff Chaikoff), aproximadamente el 14% de los pacientes manejados con este fármaco desarrollan hipotiroidismo.
El litio también puede causar hipotiroidismo, en un estudio cohorte basado en la población, el 38.6% de los pacientes necesitaron levotiroxina a los 18 meses de haberlo iniciado.
También están los fármacos antiepilépticos, fármacos de segunda línea para la tuberculosis multiresistente. Otras causas son posteriores al uso de yodo radioactivo, uso de radiación en cuello o enfermedad infiltrativa. El hipotiroidismo ocurre en el 55% de pacientes tratados con bocio nodular toxico y 8% de pacientes atendidos por nódulos solitarios.
Como causa de hipotiroidismo transitorio tenemos tiroiditis posparto, subaguda, silente y asociada con anticuerpos bloqueadores del receptor de la hormona estimulante del tiroides.
Hipotiroidismo central
Es raro y afecta a ambos sexos por igual, se asocia más que todo a trastornos hipofisiarios, pero con frecuencia involucra también al hipotálamo.
Bioquímicamente se encuentra concentraciones bajas o normales de TSH y concentración desproporcionadamente baja de tiroxina libre. La causa más frecuente son los adenomas hipofisiarios, apoplejía hipofisaria.
Hipotiroidismo periférico
Es causado por la expresión aberrante de la enzima desyodasa 3 que inactiva la hormona tiroidea en los tejidos tumorales. Es poco común, y puede provocar hipotiroidismo grave.
Presentación clínica
Su presentación va desde cuadros asintomáticos hasta cuadros que amenazan la vida. El 15% de los pacientes con problemas autoinmunes son asintomáticos o presentan escasos síntomas. La gravedad de estas manifestaciones generalmente refleja el grado de disfunción tiroidea , el tiempo de desarrollo del hipotiroidismo y pueden variar con la edad y sexo.
Los síntomas pueden ser inespecíficos, incluyen aumento de peso, fatiga, falta de concentración, depresión, dolor muscular difuso e irregularidades menstruales.
Los síntomas con alta especificidad incluyen estreñimiento, intolerancia al frio, piel seca, debilidad muscular proximal, cambios en la vos, adelgazamiento o pérdida del cabello. En pacientes mayores el deterioro cognitivo puede ser la única manifestación.


Por sistemas podemos encontrar:
-
Síntomas generales: aumento de peso leve, debilidad, cansancio, baja tolerancia al esfuerzo, somnolencia, lentitud generalizada (psicomotora y en el habla); sensación de frío, menor tolerancia a las temperaturas bajas.
-
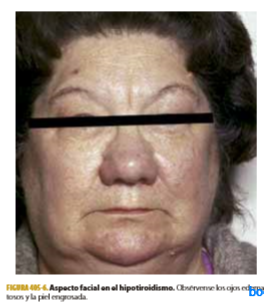
Cambios en la piel: piel seca, fría, pálida, sudoración disminuida, endurecimiento excesivo en determinadas zonas (p. ej. en los codos) edema subcutáneo (mixedema) que causa una característica hinchazón de la cara, de los párpados y de las manos; pelo seco, frágil y ralo, a veces caída de cejas.
-
Cambios en el sistema circulatorio: bradicardia, pulso y ruidos cardíacos débiles; aumento de la silueta del corazón; hipotensión, más raramente hipertensión.
-
Cambios en el aparato respiratorio: voz ronca, apagada por engrosamiento de las cuerdas vocales, macroglosia, hipopnea; infecciones de las vías espiratorias superiores y en casos graves, insuficiencia respiratoria.
-
Cambios en el aparato digestivo: estreñimiento crónico y, en casos graves, íleo; ascitis (en fases avanzadas; suelen coexistir derrame pericárdico y pleural).
-
Cambios en el aparato urinario: oliguria (riesgo de intoxicación por agua por alteración de la filtración glomerular). Si no existen edemas evidentes, estos trastornos parecen insustanciales.
-
Cambios en el sistema nervioso: mononeuropatías (p. ej. síndrome del túnel carpiano), parestesias, hiporreflexia, a veces hipoacusia.
-
Cambios en el aparato locomotor: debilidad muscular, cansancio fácil, lentitud motora, calambres musculares, mialgias; edema articular, en particular de las rodillas (engrosamiento de las membranas sinoviales y derrame sinovial).
-
Cambios en el aparato genital: en mujeres trastornos menstruales (polimenorrea, amenorrea, menorragia), infertilidad, abortos. En hombres disminución de la libido y, a veces, trastornos de la erección.
-
Trastornos psíquicos: problemas de concentración, trastornos de la memoria, depresión subclínica o establecida, inestabilidad emocional, a veces trastorno bipolar afectivo o psicosis paranoide. En casos graves se presentan demencia y coma.
En ECG es común la bradicardia, onda T aplanadas y voltaje bajo. El hipotiroidismo se ha asociado con la enfermedad hígado graso no alcohólica, mortalidad por cáncer, artritis, disfunción renal y diabetes. Los hallazgos de laboratorio pueden incluir hiponatremia, hipercapnia, hipoxia, anemia normocitica, creatinincinasa elevada, aumento del colesterol total y de las LDL.
Se puede confundir en ocasiones con un síndrome nefrótico por el edema, palidez. Muchos pacientes suelen reconocer síntomas previos cuando ya están siendo tratados.
Diagnóstico
Esta enfermedad puede persistir durante años sin diagnosticarse o confundirse con otras enfermedades. En las formas poco avanzadas es difícil hacer diagnóstico clínico, por lo que pasa desapercibida. La determinación más útil para el diagnóstico del hipotiroidismo primario es la TSH basal, que está elevada ( de 0-4-4-0 mUI/L) y T4 por debajo del rango de referencia, no hay indicación para la medición rutinaria de triyodotironina total.
Si el nivel de TSH en suero está elevado, la prueba debe repetirse con una medición de tiroxina libre en suero (T4). El hipotiroidismo primario manifiesto con un nivel elevado de TSH en suero y un nivel bajo de T4 libre en suero. Un nivel elevado de TSH en suero con un nivel de T4 libre en suero de rango normal es compatible con hipotiroidismo subclínico. Un nivel bajo de T4 libre en suero con un nivel de TSH bajo, o inapropiadamente normal, es consistente con hipotiroidismo secundario y usualmente se asociará con evidencia adicional de insuficiencia hipotálamo-hipofisaria.
La medición de anticuerpos contra peroxidasa tiroidea no es necesaria para diagnosticar la enfermedad, pero es útil para confirmar el diagnóstico de hipotiroidismo primario autoinmune.
En la USG podemos encontrar un patrón hipoecogenico , incluso en ausencia de concentraciones elevadas de anticuerpos de peroxidasa tiroidea. En ausencia de indicaciones clínicas adicionales, como palpación tiroidea anormal, no se requiere una ecografía. La medición de la tiroxina libre es importante para el diagnóstico y seguimiento del hipotiroidismo.
En la enfermedad no tiroidea provoca cambios en el metabolismo de las hormonas tiroideas, transportadores y receptores, encontrándose en los pacientes críticamente enfermos. Por lo que no debe hacerse pruebas tiroideas en estos pacientes, al menos que se considere enfermedad tiroidea o hipotiroidismo central.
La heparina, incluida la de bajo peso molecular puede dar concentraciones falsamente elevadas de la tiroxina libre.
Screening
No se recomienda realizar el cribado en la población en general, pero se debe investigar en pacientes con demencia, infertilidad, enfermedades autoinmunes, hipercolesterolemia, dismenorrea, antecedentes familiares de la enfermedad, personas que toman amiodarona, litio o por iatrogenia.
Tratamiento
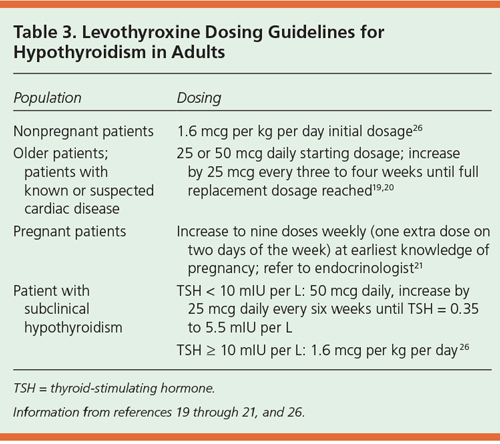
La mayoría de los pacientes con hipotiroidismo necesitarán tratamiento con hormonas tiroideas de por vida. La monoterapia con levotiroxina a dosis de 1.5-1.8 µg/kg/d es el de elección, se toma en la mañana, 30- 60 minutos antes de comer. En los ancianos se prefiere definir la dosis de 1 µg/kg/d y definir según sintomatología y concentraciones de TSH. En jóvenes sin comorbilidad se puede administrar la dosis completa con monitoreo adecuado para evitar el sobre tratamiento.
Después del inicio del tratamiento se debe repetir la TSH después de 4 a 12 semanas, luego cada 6 meses y una vez estabilizada cada año. La medición de rutina de triyodotironina no debe usarse para evaluar la efectividad del tratamiento.
Los suplementos de calcio y hierro se deben tomar después de las 4 horas de la ingesta del medicamento ya que disminuyen la absorción de la hormona tiroidea. La mala adherencia a la terapia con levotiroxina es la causa más común de niveles de TSH persistentemente elevados en pacientes que reciben dosis adecuadas de hormona tiroidea. En general la dosis debe ajustarse según la respuesta clínica y los parámetros de laboratorio.
Objetivos del tratamiento
Los objetivos son normalizar los niveles de TSH y la resolución de las molestias físicas y mentales, evitando el tratamiento insuficiente o excesivo.
Se estima que entre el 30-65% no alcanza los niveles óptimos de TSH.
Los resultados de un estudio de cohorte retrospectivo en el Reino Unido mostró que, después de 5 años de terapia con levotiroxina, casi el 6% de los pacientes tienen concentraciones de TSH por debajo de 0-1 mUI/L y más del 10% tienen concentraciones de TSH por encima de 10-0 mUI/ L.
El sobre tratamiento puede tener efectos nocivos para la salud, como fibrilación auricular y osteoporosis, y siempre debe evitarse, especialmente en las mujeres de edad avanzada y posmenopáusicas. El sub tratamiento puede resultar en un mayor riesgo de enfermedad cardiovascular y signos y síntomas persistentes. Los objetivos de tratamiento para el hipotiroidismo central son diferentes del hipotiroidismo primario porque los médicos no pueden confiar en la llamada estrategia de TSH refleja.
Caso clínico
Mujer de 80 años con antecedentes personales de hipertensión de 10 años de evolución en tratamiento con furosemida e hipercolesterolemia de 2 años de evolución en tratamiento con estatinas. En septiembre de 2003 fue diagnosticada de carcinoma epidermoide de glotis, en estadio T3N1M0, el cual fue tratado con quimioterapia y radioterapia. Una semana antes de acudir a la consulta comenzó con pérdida de memoria reciente; su familia achaca este deterioro a la senilidad. Además, en los últimos días se ha añadido una alteración de la conducta acompañada de delirios, motivo por el que se solicita la consulta. La paciente está agresiva e irritada sin causa alguna que lo justifique, desconfía de todos y admite que ha observado cómo le esconden el dinero; además, en varias ocasiones la han encontrado hablando sola. Desde hace 6 meses la paciente se fatiga al subir escaleras, ronca por las noches y presenta sensación distérmica. La exploración física sin relevancia, excepto hallazgos que sugiere deterioro cognitivo. Se realizó un hemograma, una bioquímica completa y se solicitaron pruebas de función tiroidea y se realizó un electrocardiograma. Los resultados se exponen a continuación: hemoglobina de 11 g/dl, VCM de 86 fl, HCM de 34 g/dl, y el resto de los resultados fueron completamente normales, el estudio de la función tiroidea, reportó las siguientes alteraciones: T4 libre de 0,5 µg/dl y TSH > 40 µU/ml. Los anticuerpos antimicrosomales y antitiroglobulina fueron negativos. Se inició tratamiento con levotiroxina por vía oral a dosis de 25 µg/día, con incrementos de 25 µg/día cada 2 semanas hasta alcanzar sin problemas una dosis total de 75 µg/día. Al cabo de 7 semanas de tratamiento se confirmó que la paciente estaba de nuevo en su situación basal.
Discusión y conclusiones
La paciente presentó un hipotiroidismo primario iatrógeno debido a tratamiento con radioterapia externa craneocervical.
Bibliografía
- Gaitonde DY. Rowley KD. Sweeney LB. Hypotyroidismo an update, Eisenhower Army Medical Center, Fort Gordon, Georgia.
- Jose Antonio Lozano, Hipotiroidismo, manifestaciones clínicas, diagnóstico y tratamiento, vol 25 num. 1, 2006.
- Chaker L, Bianco A, Jonklaas J et all, Hypotyroidismo , lancet 2017.
- Harrinson, Principios de Medicina Interna, 19 edición, volumen 2.
- Medicina Interna Basada en evidencia., 3° edición ; Hipotiroidismo, revisado en:
https://empendium.com/manualmibe/chapter/B34.II.9.1; abril 2021.